Jedno od važnih pitanja u proučavanju termodinamičkih sustava u fizici je pitanje može li ovaj sustav obaviti neki koristan posao. Usko vezan uz pojam rada je i pojam unutarnje energije. U ovom članku razmotrit ćemo kolika je unutarnja energija idealnog plina i dati formule za njezino izračunavanje.
Idealni plin
O plinu, kao agregacijskom stanju, koje nema nikakvu elastičnu silu pod vanjskim utjecajem na njega i zbog toga ne zadržava volumen i oblik, zna svaki školarac. Koncept idealnog plina za mnoge ostaje neshvatljiv i nejasan. Hajde da to objasnimo.
Idealni plin je svaki plin koji zadovoljava sljedeća dva važna uvjeta:
- Čestice koje ga čine nemaju veličinu. Imaju veličinu, ali je toliko mala u usporedbi s udaljenostima između njih da se može zanemariti u svim matematičkim izračunima.
- Čestice ne stupaju u interakciju jedna s drugom korištenjem van der Waalsovih sila ili siladruga priroda. Zapravo, u svim stvarnim plinovima takva je interakcija prisutna, ali je njezina energija zanemariva u usporedbi s prosječnom energijom kinetičkih čestica.
Opisanim uvjetima zadovoljavaju gotovo svi stvarni plinovi čije su temperature iznad 300 K, a pritisci ne prelaze jednu atmosferu. Za previsoke tlakove i niske temperature opaža se odstupanje plinova od idealnog ponašanja. U ovom slučaju se govori o pravim plinovima. Oni su opisani van der Waalsovom jednadžbom.
Koncept unutarnje energije idealnog plina
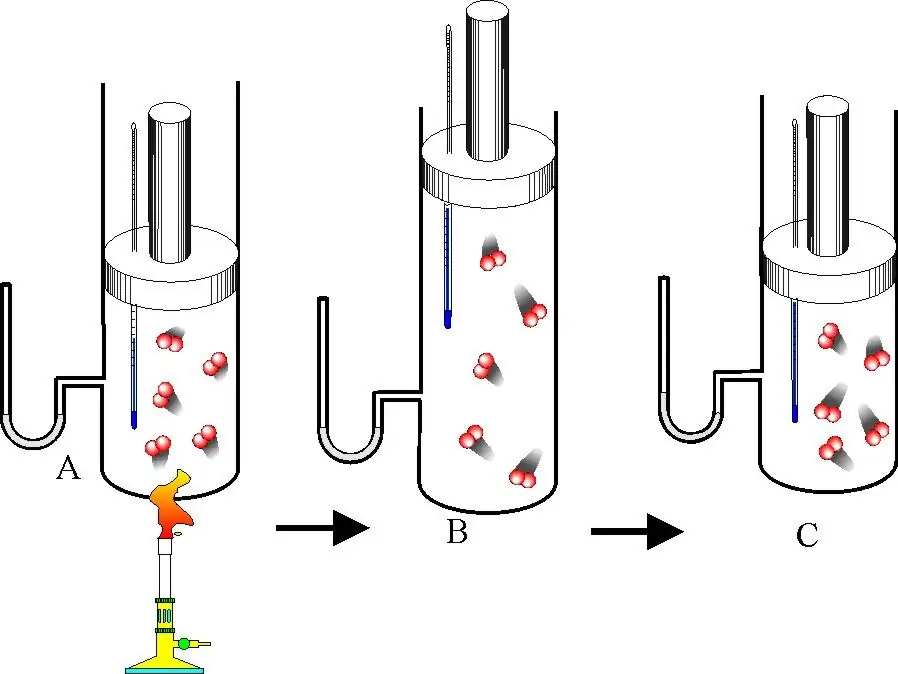
U skladu s definicijom, unutarnja energija sustava je zbroj kinetičke i potencijalne energije sadržane u ovom sustavu. Ako se ovaj koncept primjenjuje na idealni plin, tada potencijalnu komponentu treba odbaciti. Doista, budući da čestice idealnog plina ne djeluju jedna na drugu, može se smatrati da se slobodno kreću u apsolutnom vakuumu. Za izdvajanje jedne čestice iz sustava koji se proučava, nije potrebno raditi protiv unutarnjih sila interakcije, jer te sile ne postoje.
Dakle, unutarnja energija idealnog plina uvijek se podudara s njegovom kinetičkom energijom. Potonji je, pak, jedinstveno određen molarnom masom čestica sustava, njihovim brojem, kao i prosječnom brzinom translacijskog i rotacijskog gibanja. Brzina kretanja ovisi o temperaturi. Povećanje temperature dovodi do povećanja unutarnje energije, i obrnuto.
Formula zaunutarnja energija
Unutarnju energiju idealnog plinskog sustava označimo slovom U. Prema termodinamici, definira se kao razlika između entalpije H sustava i umnožaka tlaka i volumena, odnosno:
U=H - pV.
U gornjem odlomku otkrili smo da vrijednost U odgovara ukupnoj kinetičkoj energiji Eksvih čestica plina:
U=Ek.
Iz statističke mehanike, u okviru molekularne kinetičke teorije (MKT) idealnog plina, slijedi da je prosječna kinetička energija jedne čestice Ek1 jednaka sljedeća vrijednost:
Ek1=z/2kBT.
Ovdje kB i T - Boltzmannova konstanta i temperatura, z - broj stupnjeva slobode. Ukupna kinetička energija sustava Ek može se dobiti množenjem Ek1 s brojem čestica N u sustavu:
Ek=NEk1=z/2NkBT.
Tako smo dobili formulu za unutarnju energiju idealnog plina, napisanu u općem obliku u smislu apsolutne temperature i broja čestica u zatvorenom sustavu:
U=z/2NkBT.
Monatomski i poliatomski plin
Formula za U napisana u prethodnom odlomku članka nezgodna je za praktičnu primjenu, jer je teško odrediti broj čestica N. Međutim, ako uzmemo u obzir definiciju količine tvari n, onda se ovaj izraz može prepisati u prikladnijem obliku:
n=N/NA; R=NAkB=8, 314 J/(molK);
U=z/2nR T.
Broj stupnjeva slobode z ovisi o geometriji čestica koje čine plin. Dakle, za monoatomski plin, z=3, budući da se atom može samostalno kretati samo u tri smjera prostora. Ako je plin dvoatomski, tada je z=5, budući da se trima translacijskim stupnjevima slobode dodaju još dva rotirajuća stupnja slobode. Konačno, za bilo koji drugi poliatomski plin, z=6 (3 translacijska i 3 rotirajuća stupnja slobode). Imajući to na umu, možemo u sljedećem obliku napisati formule za unutarnju energiju idealnog plina jednoatomnog, dvoatomskog i poliatomskog:
U1=3/2nRT;
U2=5/2nRT;
U≧3=3nRT.
Primjer zadatka za određivanje unutarnje energije
Boca od 100 litara sadrži čisti vodik pod tlakom od 3 atmosfere. Uz pretpostavku da je vodik idealan plin pod datim uvjetima, potrebno je odrediti kolika je njegova unutarnja energija.

Gornje formule za U sadrže količinu tvari i temperaturu plina. U stanju problema o tim količinama se ne govori apsolutno ništa. Da bismo riješili problem, potrebno je prisjetiti se univerzalne Clapeyron-Mendelejevske jednadžbe. Ima izgled prikazan na slici.
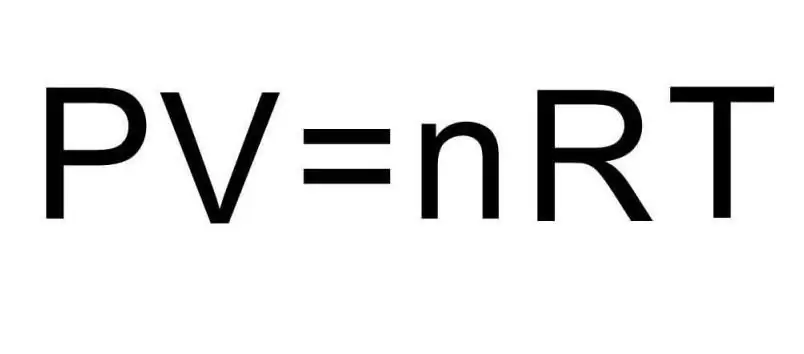
Budući da je vodik H2 dvoatomska molekula, formula za unutarnju energiju je:
UH2=5/2nRT.
Uspoređujući oba izraza, dolazimo do konačne formule za rješavanje problema:
UH2=5/2PV.
Ostaje pretvoriti jedinice tlaka i volumena iz stanja u SI sustav jedinica, zamijeniti odgovarajuće vrijednosti u formuli za UH2 i dobiti odgovor: UH2 ≈ 76 kJ.






