Termodinamika je važna grana fizike. Možemo sa sigurnošću reći da su njegova postignuća dovela do pojave tehnološke ere i uvelike odredila tijek ljudske povijesti tijekom posljednjih 300 godina. Članak govori o prvom, drugom i trećem zakonu termodinamike i njihovoj primjeni u praksi.
Što je termodinamika?
Prije formuliranja zakona termodinamike, shvatimo što radi ovaj dio fizike.
Riječ "termodinamika" grčkog je porijekla i znači "kretanje zbog topline". Odnosno, ova grana fizike bavi se proučavanjem bilo kojeg procesa, zbog čega se toplinska energija pretvara u mehaničko kretanje i obrnuto.
Osnovni zakoni termodinamike formulirani su sredinom 19. stoljeća. Znanost o "kretanju i toplini" razmatra ponašanje cijelog sustava kao cjeline, proučavajući promjenu njegovih makroskopskih parametara - temperature, tlaka i volumena, ne obraćajući pažnju na njegovu mikroskopsku strukturu. Štoviše, prvi od njih igra temeljnu ulogu u formuliranju zakonatermodinamika u fizici. Zanimljivo je primijetiti da su izvedeni isključivo iz eksperimentalnih opažanja.
Koncept termodinamičkog sustava

To znači bilo koju skupinu atoma, molekula ili drugih elemenata koji se smatraju kao cjelina. Sva tri zakona formulirana su za takozvani termodinamički sustav. Primjeri su: Zemljina atmosfera, bilo koji živi organizam, mješavina plinova u motoru s unutarnjim izgaranjem, itd.
Svi sustavi u termodinamici pripadaju jednoj od tri vrste:
- Otvoreno. Izmjenjuju i toplinu i materiju s okolinom. Na primjer, ako se hrana kuha u loncu na otvorenoj vatri, onda je ovo živopisan primjer otvorenog sustava, budući da lonac prima energiju iz vanjskog okruženja (vatre), dok sam zrači energiju u obliku topline, a iz njega također isparava voda (metabolizam).
- Zatvoreno. U takvim sustavima nema izmjene tvari s okolinom, iako dolazi do izmjene energije. Da se vratimo na prethodni slučaj: ako kuhalo za vodu pokrijete poklopcem, možete dobiti zatvoreni sustav.
- Izolirano. Ovo je vrsta termodinamičkih sustava koji ne izmjenjuju materiju ili energiju s okolnim prostorom. Primjer bi bila termosica s toplim čajem.
Termodinamička temperatura

Ovaj koncept znači kinetičku energiju čestica koje formiraju okolna tijela, što odražava brzinunasumično kretanje čestica. Što je veći, to je viša temperatura. Sukladno tome, smanjenjem kinetičke energije sustava, hladimo ga.
Ovaj koncept znači kinetičku energiju čestica koje tvore okolna tijela, što odražava brzinu kaotičnog kretanja čestica. Što je veći, to je viša temperatura. Sukladno tome, smanjenjem kinetičke energije sustava, hladimo ga.
Termodinamička temperatura izražena je u SI (Međunarodni sustav jedinica) u Kelvinima (u čast britanskog znanstvenika Williama Kelvina, koji je prvi predložio ovu ljestvicu). Razumijevanje prvog, drugog i trećeg zakona termodinamike nemoguće je bez definicije temperature.
Podjela jednog stupnja na Kelvinovoj ljestvici također odgovara jednom stupnju Celzijusa. Pretvorba između ovih jedinica provodi se prema formuli: TK =TC + 273, 15, gdje je TK i TC - temperature u kelvinima i stupnjevima Celzijusa.
Posebnost Kelvinove ljestvice je da nema negativne vrijednosti. Nula u njemu (TC=-273, 15 oC) odgovara stanju kada je toplinsko gibanje čestica sustava potpuno odsutno, čini se da su "zamrznuti".
Očuvanje energije i 1. zakon termodinamike

Godine 1824., Nicolas Léonard Sadi Carnot, francuski inženjer i fizičar, dao je hrabru sugestiju koja ne samo da je dovela do razvoja fizike, već je postala i veliki korak u poboljšanju tehnologije. Njegovomože se formulirati na sljedeći način: "Energija se ne može stvoriti ili uništiti, može se samo prenijeti iz jednog stanja u drugo."
Zapravo, izraz Sadija Carnota postulira zakon održanja energije, koji je bio temelj 1. zakona termodinamike: "Kad god sustav prima energiju izvana, on je pretvara u druge oblike, glavni od koji su toplinski i mehanički."
Matematička formula za 1. zakon je napisana na sljedeći način:
Q=ΔU + A, ovdje Q je količina topline koju okolina prenosi na sustav, ΔU je promjena unutarnje energije ovog sustava, A je savršeni mehanički rad.
Adijabatski procesi
Dobar primjer za njih je kretanje zračnih masa duž planinskih obronaka. Takve su mase ogromne (kilometri ili više), a zrak je izvrstan toplinski izolator. Navedena svojstva omogućuju nam da sve procese sa zračnim masama koji se odvijaju u kratkom vremenu smatramo adijabatskim. Kada se zrak diže uz planinsku padinu, njegov tlak pada, širi se, odnosno obavlja mehanički rad, i kao rezultat toga, hladi se. Naprotiv, kretanje zračne mase prema dolje praćeno je povećanjem tlaka u njoj, ona se komprimira i zbog toga postaje vrlo vruća.
Primjena zakona termodinamike, o kojoj je bilo riječi u prethodnom podnaslovu, najlakše se može pokazati na primjeru adijabatskog procesa.
Prema definiciji, zbog toga nema izmjene energije sokoline, odnosno u gornjoj jednadžbi, Q=0. To dovodi do sljedećeg izraza: ΔU=-A. Znak minus ovdje znači da sustav obavlja mehanički rad smanjujući vlastitu unutarnju energiju. Treba podsjetiti da je unutarnja energija izravno ovisna o temperaturi sustava.
Smjer toplinskih procesa
Ovo se izdanje bavi 2. zakonom termodinamike. Sigurno su svi primijetili da ako dovedete u kontakt dva predmeta s različitim temperaturama, onda će se hladni uvijek zagrijati, a vrući ohladiti. Imajte na umu da se obrnuti proces može dogoditi u okviru prvog zakona termodinamike, ali se nikada ne provodi u praksi.
Razlog nepovratnosti ovog procesa (i svih poznatih procesa u Svemiru) je prijelaz sustava u vjerojatnije stanje. U razmatranom primjeru s kontaktom dvaju tijela različitih temperatura, najvjerojatnije stanje će biti ono u kojem će sve čestice sustava imati istu kinetičku energiju.
Drugi zakon termodinamike može se formulirati na sljedeći način: "Toplota se nikada ne može spontano prenijeti s hladnog tijela na vruće." Ako uvedemo koncept entropije kao mjere nereda, onda se to može predstaviti na sljedeći način: "Svaki termodinamički proces se odvija s povećanjem entropije".
toplinski motor

Ovaj pojam shvaća se kao sustav koji zbog opskrbe vanjskom energijom može obavljati mehanički rad. Prvitoplinski strojevi bili su parni strojevi i izumljeni su krajem 17. stoljeća.
Drugi zakon termodinamike igra odlučujuću ulogu u određivanju njihove učinkovitosti. Sadi Carnot je također ustanovio da je maksimalna učinkovitost ovog uređaja: Učinkovitost=(T2 - T1)/T2, ovdje su T2 i T1 temperature grijača i hladnjaka. Mehanički se rad može izvesti samo kada postoji tok topline iz vrućeg tijela u hladno, a taj se tok ne može 100% pretvoriti u korisnu energiju.
Slika ispod prikazuje princip rada toplinskog motora (Qabs - toplina koja se prenosi na stroj, Qced - gubitak topline, W - korisni rad, P i V - tlak i volumen plina u klipu).
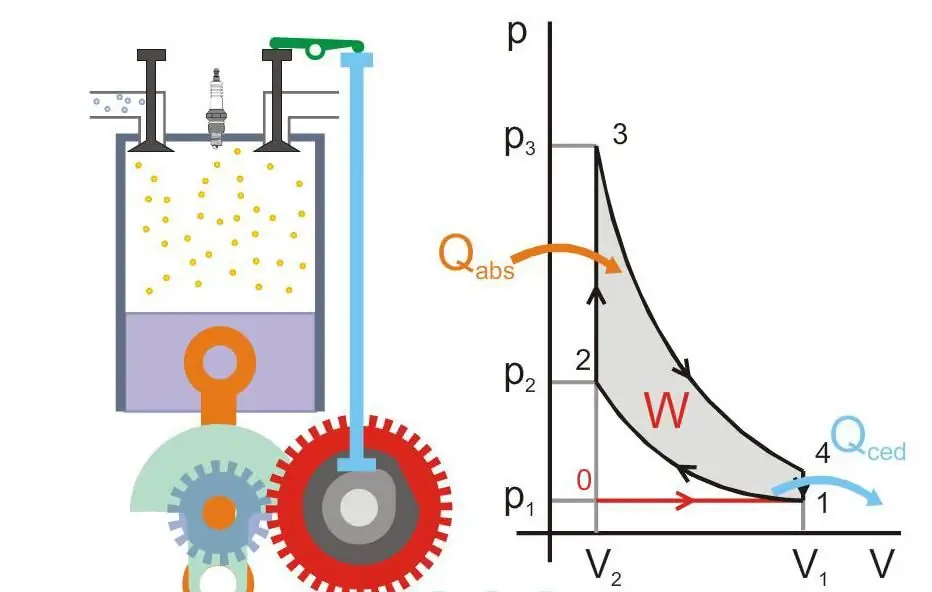
Apsolutna nula i Nernstov postulat
Na kraju, prijeđimo na razmatranje trećeg zakona termodinamike. Naziva se i Nernstov postulat (ime njemačkog fizičara koji ga je prvi formulirao početkom 20. stoljeća). Zakon kaže: "Apsolutna nula ne može se postići s konačnim brojem procesa." Odnosno, nemoguće je na bilo koji način potpuno "zamrznuti" molekule i atome tvari. Razlog tome je stalna postojeća izmjena topline s okolinom.

Jedan koristan zaključak izvučen iz trećeg zakona termodinamike je da se entropija smanjuje kako se krećemo prema apsolutnoj nuli. To znači da se sustav teži samoorganiziranju. Ova činjenica možekoristiti, na primjer, za prijenos paramagneta u feromagnetno stanje kada se ohlade.
Zanimljivo je napomenuti da je najniža temperatura koja je dosad postignuta 5·10−10 K (2003., MIT laboratorij, SAD).






