Toplinski kapacitet plina je količina energije koju tijelo apsorbira kada se zagrije za jedan stupanj. Analizirajmo glavne karakteristike ove fizičke veličine.

Definicije
Specifična toplina plina je jedinica mase određene tvari. Njegove mjerne jedinice su J/(kg·K). Količina topline koju tijelo apsorbira u procesu promjene svog agregacijskog stanja povezana je ne samo s početnim i konačnim stanjem, već i s načinom prijelaza.

Odjel
Toplinski kapacitet plinova podijeljen je s vrijednošću utvrđenom pri konstantnom volumenu (Cv), konstantnom tlaku (Cr).
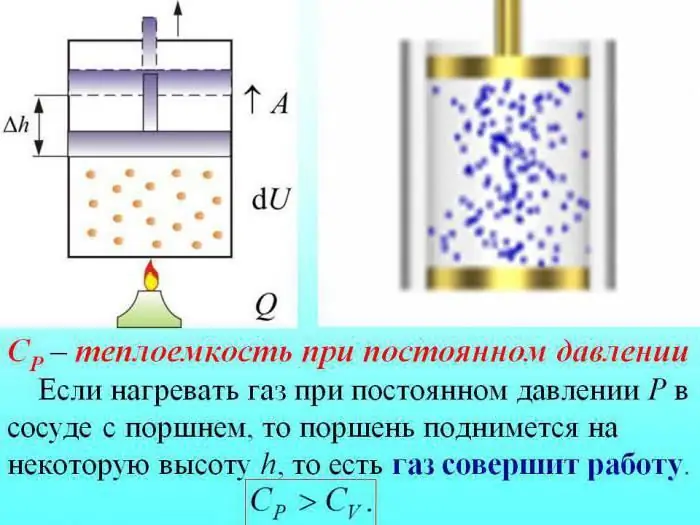
U slučaju zagrijavanja bez promjene tlaka, dio topline se troši za proizvodnju rada ekspanzije plina, a dio energije se troši na povećanje unutarnje energije.
Toplinski kapacitet plinova pri konstantnom tlaku određen je količinom topline koja se troši na povećanje unutarnje energije.
Stanje plina: značajke, opis
Toplinski kapacitet idealnog plina određuje se uzimajući u obzir činjenicu da je Sp-Sv=R. Posljednja veličina naziva se univerzalna plinska konstanta. Njegova vrijednost odgovara 8,314 J/(mol K).
Prilikom izvođenja teoretskih proračuna toplinskog kapaciteta, na primjer, opisivanja odnosa s temperaturom, nije dovoljno koristiti samo termodinamičke metode, važno je naoružati se elementima statičke fizike.
Toplinski kapacitet plinova uključuje izračun prosječne vrijednosti energije translacijskog gibanja nekih molekula. Takvo kretanje je sažeto iz rotacijskog i translacijskog kretanja molekule, kao i iz unutarnjih vibracija atoma.
U statičkoj fizici postoji informacija da za svaki stupanj slobode rotacijskog i translacijskog gibanja postoji količina plina koja je jednaka polovici univerzalne plinske konstante.

Zanimljive činjenice
Pretpostavlja se da čestica jednoatomnog plina ima tri translacijska stupnja slobode, tako da specifična toplina plina ima tri translacijska, dva rotirajuća i jedan vibracijski stupnja slobode. Zakon njihove ujednačene raspodjele dovodi do izjednačavanja specifične topline pri konstantnom volumenu s R.
Tijekom eksperimenata ustanovljeno je da toplinski kapacitet dvoatomskog plina odgovara vrijednosti R. Takvo neslaganje između teorije i prakse objašnjava se činjenicom da je toplinski kapacitet idealnog plina povezan s kvantnim učinke, stoga je pri izračunima važno koristiti statistiku koja se temelji na kvantimamehanika.
Utemeljen na temeljima kvantne mehanike, svaki sustav čestica koji osciliraju ili rotiraju, uključujući molekule plina, ima samo neke diskretne vrijednosti energije.
Ako energija toplinskog gibanja u sustavu nije dovoljna da potakne oscilacije određene frekvencije, takva gibanja ne doprinose ukupnom toplinskom kapacitetu sustava.
Kao rezultat toga, određeni stupanj slobode postaje "zamrznut", na njega je nemoguće primijeniti zakon jednake podjele.
Toplinski kapacitet plinova važna je karakteristika stanja o kojem ovisi funkcioniranje cjelokupnog termodinamičkog sustava.
Temperatura na kojoj se zakon ravnomjerne raspodjele može primijeniti na vibracijski ili rotacijski stupanj slobode karakterizira kvantna teorija, povezuje Planckovu konstantu s Boltzmannovom konstantom.

Dijatomski plinovi
Razzori između razina rotacijske energije takvih plinova su mali broj stupnjeva. Iznimka je vodik u kojem je vrijednost temperature određena stotinama stupnjeva.
Zato je toplinski kapacitet plina pri konstantnom tlaku teško opisati zakonom jednolike raspodjele. U kvantnoj statistici, pri određivanju toplinskog kapaciteta, uzima se u obzir da se njegov vibracijski dio, u slučaju pada temperature, brzo smanjuje i doseže nulu.
Ovaj fenomen objašnjava činjenicu da na sobnoj temperaturi praktički nema vibracijskog dijela toplinskog kapaciteta, zadvoatomski plin, odgovara konstanti R.
Toplinski kapacitet plina pri konstantnom volumenu u slučaju niskotemperaturnih indikatora određuje se pomoću kvantne statistike. Postoji Nernstov princip, koji se zove treći zakon termodinamike. Na temelju njegove formulacije, molarni toplinski kapacitet plina smanjit će se s padom temperature, težeći nuli.

Značajke čvrste tvari
Ako se toplinski kapacitet mješavine plinova može objasniti kvantnom statistikom, tada je za čvrsto stanje agregacije toplinsko gibanje karakterizirano blagim fluktuacijama čestica u blizini ravnotežnog položaja.
Svaki atom ima tri vibracijska stupnja slobode, stoga, u skladu sa zakonom ekviparticije, molarni toplinski kapacitet čvrste tvari može se izračunati kao 3nR, pri čemu je n broj atoma u molekuli.
U praksi, ovaj broj je granica kojoj teži toplinski kapacitet čvrstog tijela pri visokim temperaturama.
Maksimum se može dobiti na uobičajenim temperaturama za neke elemente, uključujući metale. Za n=1 Dulongov i Petitov zakon je ispunjen, ali je za složene tvari prilično teško doći do takve granice. Budući da se granica u stvarnosti ne može postići, dolazi do raspadanja ili topljenja krutine.
Povijest kvantne teorije
Osnivači kvantne teorije su Einstein i Debye na početku dvadesetog stoljeća. Temelji se na kvantizaciji oscilatornih gibanja atoma u određenomkristal. U slučaju niskotemperaturnih pokazatelja, toplinski kapacitet čvrstog tijela pokazuje se da je izravno proporcionalan apsolutnoj vrijednosti uzetoj u kockama. Ovaj odnos je nazvan Debyeov zakon. Kao kriterij koji omogućuje razlikovanje indikatora niske i visoke temperature uzima se njihova usporedba s Debye temperaturom.
Ova vrijednost je određena spektrom vibracija atoma u tijelu, stoga ozbiljno ovisi o značajkama njegove kristalne strukture.
QD je vrijednost koja ima nekoliko stotina K, ali je, na primjer, mnogo veća u dijamantu.
Elektroni vodljivosti daju značajan doprinos toplinskom kapacitetu metala. Za njegovo izračunavanje koristi se Fermijeva kvantna statistika. Elektronska vodljivost za atome metala izravno je proporcionalna apsolutnoj temperaturi. Budući da je to beznačajna vrijednost, uzima se u obzir samo pri temperaturama koje teže apsolutnoj nuli.
Metode za određivanje toplinskog kapaciteta
Glavna eksperimentalna metoda je kalorimetrija. Za teorijski proračun toplinskog kapaciteta koristi se statistička termodinamika. Vrijedi za idealni plin, kao i za kristalna tijela, provodi se na temelju eksperimentalnih podataka o strukturi materije.
Empirijske metode za izračunavanje toplinskog kapaciteta idealnog plina temelje se na ideji kemijske strukture, doprinosa pojedinih skupina atoma Sr.
Za tekućine se također koriste metode koje se temelje na upotrebi termodinamikeciklusi koji omogućuju prijelaz iz toplinskog kapaciteta idealnog plina u tekućinu kroz derivaciju temperature entalpije procesa isparavanja.
U slučaju otopine, izračun toplinskog kapaciteta kao aditivne funkcije nije dopušten, budući da je višak vrijednosti toplinskog kapaciteta otopine u osnovi značajan.
Da bismo to procijenili, potrebna nam je molekularno-statistička teorija otopina. Najteže je identificirati toplinski kapacitet heterogenih sustava u termodinamičkoj analizi.

Zaključak
Proučavanje toplinskog kapaciteta omogućuje vam izračunavanje energetske ravnoteže procesa koji se odvijaju u kemijskim reaktorima, kao iu drugim aparatima za kemijsku proizvodnju. Osim toga, ova vrijednost je neophodna za odabir optimalnih vrsta rashladnih tekućina.
Trenutno je eksperimentalno određivanje toplinskog kapaciteta tvari za različite temperaturne intervale - od niskih vrijednosti do visokih vrijednosti - glavna opcija za određivanje termodinamičkih karakteristika tvari. Pri izračunavanju entropije i entalpije tvari koriste se integrali toplinskog kapaciteta. Informacije o toplinskom kapacitetu kemijskih reagensa u određenom temperaturnom rasponu omogućuju vam izračunavanje toplinskog učinka procesa. Podaci o toplinskom kapacitetu otopina omogućuju izračunavanje njihovih termodinamičkih parametara pri bilo kojoj vrijednosti temperature unutar analiziranog intervala.
Na primjer, tekućinu karakterizira utrošak dijela topline za promjenu vrijednosti potencijalne energijemolekule koje reagiraju. Ova vrijednost naziva se toplinskim kapacitetom "konfiguracije", koristi se za opisivanje rješenja.
Teško je provesti potpune matematičke izračune bez uzimanja u obzir termodinamičkih karakteristika tvari, njezinog agregacijskog stanja. Zato se za tekućine, plinove, krute tvari koristi takva karakteristika kao što je specifični toplinski kapacitet, što omogućuje karakterizaciju energetskih parametara tvari.






