Proučavanje svojstava idealnog plina važna je tema u fizici. Uvod u karakteristike plinskih sustava počinje razmatranjem Boyle-Mariotteove jednadžbe, budući da je to prvi eksperimentalno otkriven zakon idealnog plina. Razmotrimo to detaljnije u članku.
Što se podrazumijeva pod idealnim plinom?
Prije nego što počnemo govoriti o Boyle-Mariotteovom zakonu i jednadžbi koja ga opisuje, definirajmo idealni plin. Uobičajeno se shvaća kao fluidna tvar u kojoj čestice koje ga čine ne djeluju jedna na drugu, a njihove su veličine zanemarivo male u usporedbi s prosječnim međučestičnim udaljenostima.
Zapravo, svaki plin je stvaran, to jest, njegovi sastavni atomi i molekule imaju određenu veličinu i ne stupaju u interakciju jedni s drugima uz pomoć van der Waalsovih sila. Međutim, pri visokim apsolutnim temperaturama (više od 300 K) i niskim tlakovima (manje od jedne atmosfere), kinetička energija atoma i molekula je puno veća od energije van der Waalsovih interakcija, pa je pravi plin na naznačenojuvjeti s visokom preciznošću mogu se smatrati idealnim.
Boyle-Mariotteova jednadžba
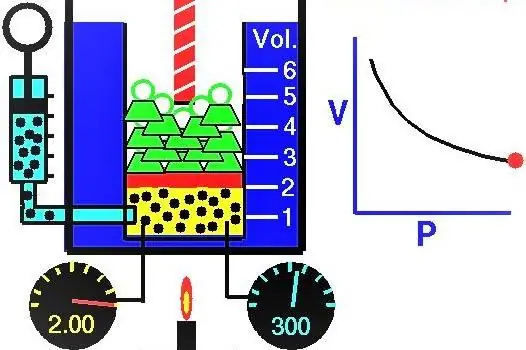
Svojstva plinova europski su znanstvenici aktivno istraživali tijekom XVII-XIX stoljeća. Prvi plinski zakon koji je eksperimentalno otkriven bio je zakon koji opisuje izotermne procese širenja i kompresije plinskog sustava. Odgovarajuće pokuse izveli su Robert Boyle 1662. i Edm Mariotte 1676. godine. Svaki od ovih znanstvenika nezavisno je pokazao da se tijekom izotermnog procesa u zatvorenom plinskom sustavu tlak mijenja obrnuto s volumenom. Eksperimentalno dobiveni matematički izraz procesa zapisuje se u sljedećem obliku:
PV=k
Gdje su P i V tlak u sustavu i njegov volumen, k je neka konstanta čija vrijednost ovisi o količini plinovite tvari i njezinoj temperaturi. Ako gradite ovisnost funkcije P(V) na grafu, onda će to biti hiperbola. Primjer ovih krivulja prikazan je u nastavku.
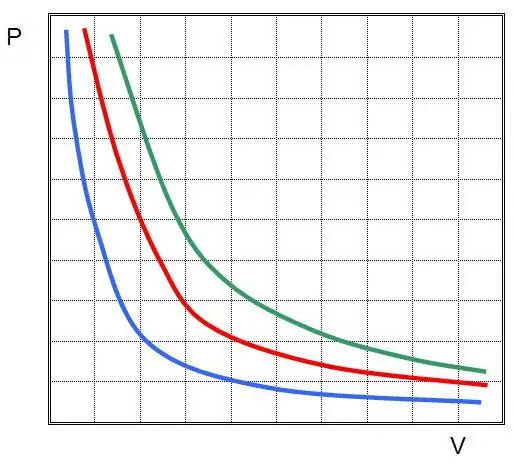
Napisana jednakost naziva se Boyle-Mariotteova jednadžba (zakon). Ovaj se zakon može ukratko formulirati na sljedeći način: širenje idealnog plina pri konstantnoj temperaturi dovodi do proporcionalnog smanjenja tlaka u njemu, naprotiv, izotermni kompresija plinskog sustava popraćena je proporcionalnim povećanjem tlaka u njemu.
Idealna plinska jednadžba
Boyle-Mariotteov zakon je poseban slučaj općenitijeg zakona koji nosi imena Mendelejeva iClapeyron. Emile Clapeyron, sažimajući eksperimentalne informacije o ponašanju plinova u različitim vanjskim uvjetima, 1834. godine dobio je sljedeću jednadžbu:
PV=nRT
Drugim riječima, umnožak volumena V plinskog sustava i tlaka P u njemu izravno je proporcionalan umnošku apsolutne temperature T i količine tvari n. Koeficijent ove proporcionalnosti označava se slovom R i naziva se plinska univerzalna konstanta. U napisanoj jednadžbi, vrijednost R se pojavila zbog zamjene niza konstanti, koju je napravio Dmitrij Ivanovič Mendeljejev 1874.
Iz univerzalne jednadžbe stanja lako je vidjeti da konstantnost temperature i količine tvari jamči nepromjenjivost desne strane jednadžbe, što znači da će i lijeva strana jednadžbe ostati konstantna. U ovom slučaju, dobivamo Boyle-Mariotteovu jednadžbu.

Drugi zakoni o plinu
Clapeyron-Mendeleev jednadžba napisana u gornjem odlomku sadrži tri termodinamička parametra: P, V i T. Ako je svaki od njih fiksiran, a druga dva se smiju mijenjati, tada ćemo dobiti Boyle-Mariotte, Charlesove i Gay-Lussacove jednadžbe. Charlesov zakon govori o izravnoj proporcionalnosti između volumena i temperature za izobarični proces, a Gay-Lussacov zakon kaže da se u slučaju izohornog prijelaza tlak plina povećava ili smanjuje izravno proporcionalno apsolutnoj temperaturi. Odgovarajuće jednadžbe izgledaju ovako:
V/T=const kada je P=const;
P/T=konst kada je V=konst.
DakleDakle, Boyle-Mariotteov zakon je jedan od tri glavna plinska zakona. Međutim, razlikuje se od ostalih u smislu grafičke ovisnosti: funkcije V(T) i P(T) su ravne linije, funkcija P(V) je hiperbola.
Primjer zadatka za primjenu Boyle-Mariotteovog zakona
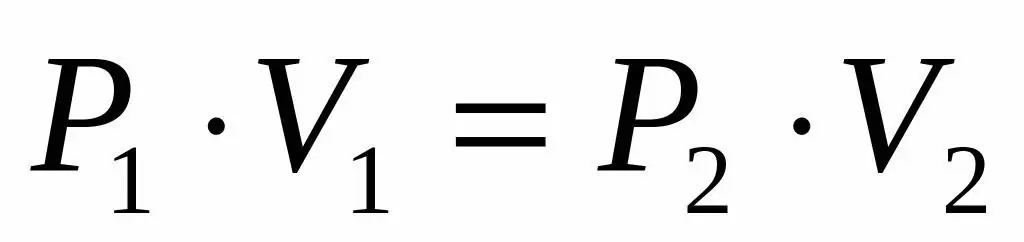
Zapremina plina u cilindru ispod klipa u početnom položaju iznosila je 2 litre, a tlak 1 atmosfera. Koliki je bio tlak plina nakon podizanja klipa i povećanja volumena plinskog sustava za 0,5 litara. Proces se smatra izotermnim.
Budući da nam je dan tlak i volumen idealnog plina, a također znamo da temperatura ostaje nepromijenjena tijekom njegovog širenja, možemo koristiti Boyle-Mariotteovu jednadžbu u sljedećem obliku:
P1V1=P2V 2
Ova jednakost kaže da je umnožak volumen-tlak konstantan za svako stanje plina na danoj temperaturi. Izražavajući vrijednost P2 iz jednakosti, dobivamo konačnu formulu:
P2=P1V1/V 2
Kada radite izračune tlaka, u ovom slučaju možete koristiti jedinice izvan sustava, jer će se litre smanjiti, a tlak P2 dobivamo u atmosferama. Zamjenom podataka iz uvjeta dolazimo do odgovora na pitanje zadatka: P2=0,8 atmosfera.






